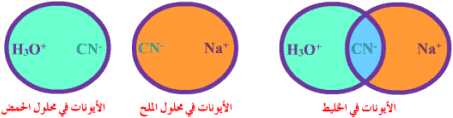
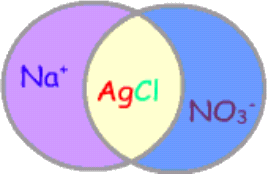
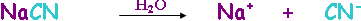أرجو أن أكون قد أفدتكم
للمشرفين : أرجو التثبيت للإفادة
Download Test :
-
 الإمتحان التجريبي 2022-2011 الكيمياء.zip (653.0 كيلوبايت, 2281 مشاهدات)
الإمتحان التجريبي 2022-2011 الكيمياء.zip (653.0 كيلوبايت, 2281 مشاهدات)
تسسلم عالامتحان اخوي..
يثبت للاهمية وان شاء الله تعم الفائدة عالجميع
اخووي استفااد كتييير
тнаиќ џоu
 بارك الله فيكم
بارك الله فيكم



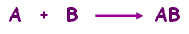
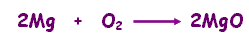









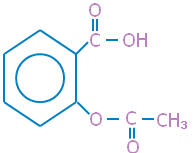
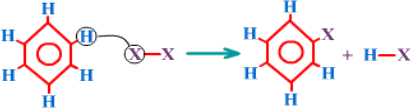


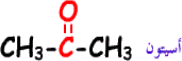



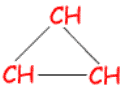

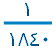 من كتلة البروتون أو النيوترون تقريباً .
من كتلة البروتون أو النيوترون تقريباً .